Contoh Soal Pilihan Ganda Laju Reaksi Kimia Dan Jawabannya
Pada kesempatan kali ini kita akan membagikan kumpulan soal pilihan ganda laju reaksi dan kunci jawaban kelas 11 SMA atau SMK. Pada materi laju reaksi, di pelajaran kimia memang yang namanya mengerjakan latihan soal adalah hal yang begitu berguna. Karena rumus akan lebih mudah di hafal apabila ada kebiasaan mengerjakannya.
Dan dengan adanya contoh soal kimia pilihan ganda berikut ini maka diharapkan para siswa dapat belajar mengerjakan soal - soal latihan dirumah ataupun sebagai persiapan menghadapi tes semesteran ataupun ulangan harian yang akan dilakukan.
Berikut ini 15 contoh soal pilihan ganda kimia tentang laju reaksi beserta jawabannya :
1. ) Seorang siswa sma mengambil 50 mL HNO3 (Mr = 63) pekat dengan kadar 31,5% dan memiliki massa jenis 1,3 g/mL. Kemudian cairan tersebut ditambahkan air hingga volumenya menjadi 750 mL. Tentukan berapa konsentrasi larutan tersebut dalam molar (M) setelah pengenceran!
a. 0,41 M
b. 0,42 M
c. 0,43 M
d. 0,44 M
e. 0,45 M
2. ) Seorang guru smk negeri mereaksikan gas nitrogen dan gas hidrogen dengan persamaan reaksi sebagai berikut:
N2 (g) + 3H2 (g) → 2NH3 (g)
Setelah melalui beberapa tahapan reaksi, dapat diketahui reaksi tersebut memiliki persamaan laju v = 0,02
Jika dalam volume 1 L direaksikan dengan 2 mol N2 dan 5 mol H2, berapakah laju reaksi setelah 75% N2 bereaksi?
a. 0,025 M/detik
b. 0,135 M/detik
c. 0,351 M/detik
d. 0,531 M/detik
e. 1,035 M/detik
3. ) Bosch dan Haber menemukan bahwa penggunaan katalis besi dengan beberapa promotor akan meningkatkan efisiensi produksi ammonia hingga 97% namun dengan biaya yang rendah. Manakah yang bukan merupakan promotor tersebut?
a. Al2O3
b. SiO2
c. K2O
d. H2O
e. CaO
4. ) Suatu reaksi 2A + B → 2C, dimulai dengan konsentrasi awal A dan B masing-masing 3 mol dan 2 mol berlangsung dalam ruang bervolume 1 liter. Jika persamaan laju reaksinya, v = 2x 10²[A]²[B], maka laju konsentrasi ketika konsentrasi A = 1 mol/L, adalah...
a. 10 M/detik
b. 50 M/detik
c. 100 M/detik
d. 150 M/detik
e. 200 M/detik
5. ) Sekelompok siswa SMAN 1 Bogor mengamati reaksi dekomposisi 20 gram PCl5 menjadi PCl3 dan gas klorin dalam wadah 2 L, dengan persamaan reaksi :
PCl5 (g) → PCl3 (g) + Cl2 (g)
Dari hasil pengamatan, ternyata dibutuhkan 25 detik untuk menghabiskan 75% PCl5. Berapa laju reaksi saat 75% PCl5 bereaksi? (Mr PCl5 = 208 gr/mol)
a. 1,44 × 10^-3 M/detik
b. 2,44 × 10^-3 M/detik
c. 3,44 × 10^-3 M/detik
d. 4,44 × 10^-3 M/detik
e. 5,44 × 10^-3 M/detik
6. ) Perhatikan proses pembuatan asam sulfat dengan katalis V2O5 berikut ini :
1.S (s) + O2 (g) → SO2 (g)
2. 2 SO2 (g) + O2(g) ⇆ 2 SO3 (g)
3. 2SO2 + 4V5+ + 2O–2 → 2SO3 + 4V4+
4. 4V4+ + O2 → 4V5+ + 2O–2SO3 (g) + 5. H2SO4 (ℓ) → H2S2O7 (ℓ)
6. H2S2O7 (ℓ) + H2O (ℓ) → H2SO4 (ℓ)
Urutan tahap reaksi yang benar adalah…
a. 1,2,3,4,5,6
b. 1,2,4,5,6,3
c. 1,6,4,2,3,5
d. 6,1,5,2,3,4
e. 4,2,3,1,5,6
7. ) Sejumlah zat tertentu HCl direaksikan dengan logam Zn akan menghasilkan H2 dan NaCl. Berdasarkan reaksi diatas, percobaan mana yang berlangsung sangat cepat pada konsentrasi HCl yang berbeda dibawah ini?
a. 0,1 M
b. 0,2 M
c. 0,3 M
d. 0,4 M
e. 0,5 M
8. ) Diketahui kondisi zat yang bereaksi sebagai berikut:
1. Serbuk seng + HCl 0,1 M
2. Lempeng seng + HCl 0,1 M
3. Serbuk seng + HCl 0,5 M
4. Butiran seng + HCl 0,5 M
5. Lempeng seng + HCl 0,5 M
Dari kondisi tersebut, reaksi yang paling cepat adalah....
a. 1
b. 2
c. 3
d. 4
e. 5
9. ) Jika suatu reaksi dinaikkan 10°C, maka laju reaksinya menjadi dua kali lebih besar. Jika pada suhu t°C reaksi berlangsung dalam waktu 4 menit pada suhu (t + 30)°C, maka reaksi tersebut akan berlangsung selama berapa menit?
a. 32 menit
b. 16 menit
c. 8 menit
d. ½ menit
e. ¼ menit
10. ) Apabila 4 gram NaOH (M=40) dilarutkan kedalam air hingga volumenya menjadi 500ml, maka kemolaran NaOH adalah...
a. 0,1
b. 0,2
c. 0,3
d. 0,4
e. 0,5
11. ) Diketahui reaksi peruraian hidrogen peroksida (H2O2) sebagai berikut:
H2O2 + 1^- →H2O + 10^-
10^- + H2O2 → H2O + O2 + 1^-
Reaksi diatas bertambah cepat ketika ditambahkan minyak katalis. Katalisator yang dimaksud adalah....
a. H2O2
b. 1^-
c. 10^-
d. H2O2 dan H2
e. 1^- dan 10^-
12. ) Dengan mereaksikan:
P2(g) + Q2(g) → 2PQ
Menghasilkan data sebagai berikut:
Apabika [P2] meningkat 2 kali lipat, [Q2] tetap, laju reaksi menjadi 4 kali dari laju reaksi semula, sementara jika [P2] dan [Q2] masing-masing meningkat 2 kali, maka laju reaksinya menjadi 8 kali, maka orde terhadap [Q2] adalah.....
a. 0
b. 32
c. 1
d. 52
e. 2
13. ) Kecepatan reaksi suatu reaksi bertambah 2 kali lipat untuk tiap kenaikan 10°C. Berapa kali lebih cepat reaksi tersebut akan berlangsung pada suhu 80°C dibanding 20°C?
a. 16 kali
b. 32 kali
c. 64 kali
d. 128 kali
e. 256 kali
14. ) Suatu persamaan pada laju reaksi untuk reaksi P + 2Q → C adalah v = K[A][B]². Apabila zat A dan zat B masing-masing memiliki konsentrasi awal 1 mol/liter, maka pada saat konsentrasi P tersisa 3/4 mol / liter. Sehingga, laju reaksinya menjadi berapa Kelvin?
a. 9/8 k
b. 3/16 k
c. 1/16 k
d. 3/8 k
e. 1/8 k
15. ) Reaksi 2NO (g) + Cl2 (g) → 2NOCl (g) adalah orde 2 terhadap NO dan 1 terhadap Cl2 dan K = 0,4 mol^-2L^2S^-1. Jika mula² gas NO dan Cl2 masing-masing adalah 3 mol dalam ruang 3 L, maka besarnya laju reaksi (M s^-1) setelah 20% dan NO terurai adalah...
a. 0,0768
b. 0,1922
c. 0,1152
d. 0,2536
e. 0,2304
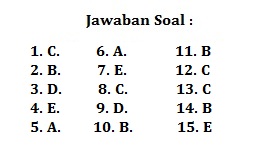
Kunci jawabannya mengenai soal soal diatas adalah dibawah ini.
Dan dengan adanya contoh soal kimia pilihan ganda berikut ini maka diharapkan para siswa dapat belajar mengerjakan soal - soal latihan dirumah ataupun sebagai persiapan menghadapi tes semesteran ataupun ulangan harian yang akan dilakukan.
Berikut ini 15 contoh soal pilihan ganda kimia tentang laju reaksi beserta jawabannya :
1. ) Seorang siswa sma mengambil 50 mL HNO3 (Mr = 63) pekat dengan kadar 31,5% dan memiliki massa jenis 1,3 g/mL. Kemudian cairan tersebut ditambahkan air hingga volumenya menjadi 750 mL. Tentukan berapa konsentrasi larutan tersebut dalam molar (M) setelah pengenceran!
a. 0,41 M
b. 0,42 M
c. 0,43 M
d. 0,44 M
e. 0,45 M
2. ) Seorang guru smk negeri mereaksikan gas nitrogen dan gas hidrogen dengan persamaan reaksi sebagai berikut:
N2 (g) + 3H2 (g) → 2NH3 (g)
Setelah melalui beberapa tahapan reaksi, dapat diketahui reaksi tersebut memiliki persamaan laju v = 0,02
Jika dalam volume 1 L direaksikan dengan 2 mol N2 dan 5 mol H2, berapakah laju reaksi setelah 75% N2 bereaksi?
a. 0,025 M/detik
b. 0,135 M/detik
c. 0,351 M/detik
d. 0,531 M/detik
e. 1,035 M/detik
3. ) Bosch dan Haber menemukan bahwa penggunaan katalis besi dengan beberapa promotor akan meningkatkan efisiensi produksi ammonia hingga 97% namun dengan biaya yang rendah. Manakah yang bukan merupakan promotor tersebut?
a. Al2O3
b. SiO2
c. K2O
d. H2O
e. CaO
4. ) Suatu reaksi 2A + B → 2C, dimulai dengan konsentrasi awal A dan B masing-masing 3 mol dan 2 mol berlangsung dalam ruang bervolume 1 liter. Jika persamaan laju reaksinya, v = 2x 10²[A]²[B], maka laju konsentrasi ketika konsentrasi A = 1 mol/L, adalah...
a. 10 M/detik
b. 50 M/detik
c. 100 M/detik
d. 150 M/detik
e. 200 M/detik
5. ) Sekelompok siswa SMAN 1 Bogor mengamati reaksi dekomposisi 20 gram PCl5 menjadi PCl3 dan gas klorin dalam wadah 2 L, dengan persamaan reaksi :
PCl5 (g) → PCl3 (g) + Cl2 (g)
Dari hasil pengamatan, ternyata dibutuhkan 25 detik untuk menghabiskan 75% PCl5. Berapa laju reaksi saat 75% PCl5 bereaksi? (Mr PCl5 = 208 gr/mol)
a. 1,44 × 10^-3 M/detik
b. 2,44 × 10^-3 M/detik
c. 3,44 × 10^-3 M/detik
d. 4,44 × 10^-3 M/detik
e. 5,44 × 10^-3 M/detik
6. ) Perhatikan proses pembuatan asam sulfat dengan katalis V2O5 berikut ini :
1.S (s) + O2 (g) → SO2 (g)
2. 2 SO2 (g) + O2(g) ⇆ 2 SO3 (g)
3. 2SO2 + 4V5+ + 2O–2 → 2SO3 + 4V4+
4. 4V4+ + O2 → 4V5+ + 2O–2SO3 (g) + 5. H2SO4 (ℓ) → H2S2O7 (ℓ)
6. H2S2O7 (ℓ) + H2O (ℓ) → H2SO4 (ℓ)
Urutan tahap reaksi yang benar adalah…
a. 1,2,3,4,5,6
b. 1,2,4,5,6,3
c. 1,6,4,2,3,5
d. 6,1,5,2,3,4
e. 4,2,3,1,5,6
7. ) Sejumlah zat tertentu HCl direaksikan dengan logam Zn akan menghasilkan H2 dan NaCl. Berdasarkan reaksi diatas, percobaan mana yang berlangsung sangat cepat pada konsentrasi HCl yang berbeda dibawah ini?
a. 0,1 M
b. 0,2 M
c. 0,3 M
d. 0,4 M
e. 0,5 M
8. ) Diketahui kondisi zat yang bereaksi sebagai berikut:
1. Serbuk seng + HCl 0,1 M
2. Lempeng seng + HCl 0,1 M
3. Serbuk seng + HCl 0,5 M
4. Butiran seng + HCl 0,5 M
5. Lempeng seng + HCl 0,5 M
Dari kondisi tersebut, reaksi yang paling cepat adalah....
a. 1
b. 2
c. 3
d. 4
e. 5
9. ) Jika suatu reaksi dinaikkan 10°C, maka laju reaksinya menjadi dua kali lebih besar. Jika pada suhu t°C reaksi berlangsung dalam waktu 4 menit pada suhu (t + 30)°C, maka reaksi tersebut akan berlangsung selama berapa menit?
a. 32 menit
b. 16 menit
c. 8 menit
d. ½ menit
e. ¼ menit
10. ) Apabila 4 gram NaOH (M=40) dilarutkan kedalam air hingga volumenya menjadi 500ml, maka kemolaran NaOH adalah...
a. 0,1
b. 0,2
c. 0,3
d. 0,4
e. 0,5
11. ) Diketahui reaksi peruraian hidrogen peroksida (H2O2) sebagai berikut:
H2O2 + 1^- →H2O + 10^-
10^- + H2O2 → H2O + O2 + 1^-
Reaksi diatas bertambah cepat ketika ditambahkan minyak katalis. Katalisator yang dimaksud adalah....
a. H2O2
b. 1^-
c. 10^-
d. H2O2 dan H2
e. 1^- dan 10^-
12. ) Dengan mereaksikan:
P2(g) + Q2(g) → 2PQ
Menghasilkan data sebagai berikut:
Apabika [P2] meningkat 2 kali lipat, [Q2] tetap, laju reaksi menjadi 4 kali dari laju reaksi semula, sementara jika [P2] dan [Q2] masing-masing meningkat 2 kali, maka laju reaksinya menjadi 8 kali, maka orde terhadap [Q2] adalah.....
a. 0
b. 32
c. 1
d. 52
e. 2
13. ) Kecepatan reaksi suatu reaksi bertambah 2 kali lipat untuk tiap kenaikan 10°C. Berapa kali lebih cepat reaksi tersebut akan berlangsung pada suhu 80°C dibanding 20°C?
a. 16 kali
b. 32 kali
c. 64 kali
d. 128 kali
e. 256 kali
14. ) Suatu persamaan pada laju reaksi untuk reaksi P + 2Q → C adalah v = K[A][B]². Apabila zat A dan zat B masing-masing memiliki konsentrasi awal 1 mol/liter, maka pada saat konsentrasi P tersisa 3/4 mol / liter. Sehingga, laju reaksinya menjadi berapa Kelvin?
a. 9/8 k
b. 3/16 k
c. 1/16 k
d. 3/8 k
e. 1/8 k
15. ) Reaksi 2NO (g) + Cl2 (g) → 2NOCl (g) adalah orde 2 terhadap NO dan 1 terhadap Cl2 dan K = 0,4 mol^-2L^2S^-1. Jika mula² gas NO dan Cl2 masing-masing adalah 3 mol dalam ruang 3 L, maka besarnya laju reaksi (M s^-1) setelah 20% dan NO terurai adalah...
a. 0,0768
b. 0,1922
c. 0,1152
d. 0,2536
e. 0,2304
Kunci jawabannya mengenai soal soal diatas adalah dibawah ini.
Demikianlah kumpulan contoh soal pilihan ganda tentang laju reaksi dan jawaban kelas 11. Semoga bermnfaat dan selamat mengerjakannya.


Post a Comment for "Contoh Soal Pilihan Ganda Laju Reaksi Kimia Dan Jawabannya "